IF-PB (Instituto Federal de Educação, Ciência e Tecnologia da Paraíba) - Professor EBTT - Química - IDECAN (Instituto de Desenvolvimento Educacional, Cultural e Assistencial Nacional) - 2019
IF-PB (Instituto Federal de Educação, Ciência e Tecnologia da Paraíba) - Professor EBTT - Química - IDECAN (Instituto de Desenvolvimento Educacional, Cultural e Assistencial Nacional) - 2019
200 g de hidrogênio molecular (H2) em condições de gás real são colocados em um cilindro de raio 50 cm e altura 100 cm. A temperatura interior do cilindro é – 182° C. A pressão deste gás no sistema, nestas condições, será aproximadamente
(Dados: PM: H=1,0 g/mol; R=0,08206 atmL/molK; a=0,244 L² atm/mol² ; b=0,02661 L/mol.)
|
a) 0,99 atm.
|
|
b) 1,2 atm.
|
|
c)
11,44 * 10-3 atm. |
|
d) 1,1 atm.
|
|
e) 0,90 atm.
|
Um experimento muito usado nas demonstrações de equilíbrio dinâmico é a mistura de NO2 e N2O4 . Este último é um gás que se liquefaz a 21ºC e congela a -11ºC, dímero do primeiro, o monômero. Considere a reação do monômero (2 mol/L) resultando no dímero (1 mol/L) em condições normais de temperatura e pressão e assinale a alternativa que indica o valor correto de Kc nessas condições.
|
a) 0,25
|
|
b) 0,50
|
|
c) 2,50
|
|
d) 2,00
|
|
e) 4,00
|
A equação obtida a partir da relação entre as equações de Planck e de Balmer-Bohr que pode ser usada para calcular a energia associada ao salto quântico de elétrons mediante a sua excitação energética e que melhor expressa o salto de um elétron da primeira camada para a quarta camada eletrônica de um certo átomo e que foi responsável por emissão de luz de um comprimento especifico de onda. Sabendo-se que h representa a constante de Planck; c , a velocidade da luz e Rh a constante de Rydberg, a equação adequada será:
|
a) E = (16/15)*Rh * c * h
|
|
b) E = (15/16)*Rh * c * h
|
|
c) E = 2,18 *Rh * c * h
|
|
d) E = 2,18 x 10 -18 *Rh * c * h
|
|
e) E = Rh * c * h
|
baixo tem-se a estrutura de argilomineral do tipo esmectita. A vermiculita é um argilomineral que se enquadra neste grupo.
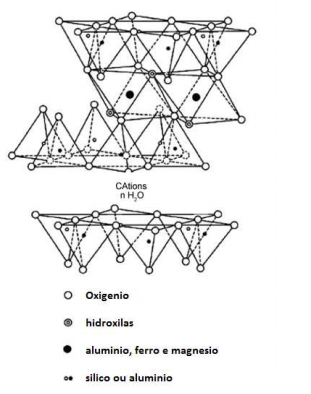
Sua formula química é dada por:
MX , (Si +45,7 Al+32,3) (Al+30,5 Mg +24,8 Fe+30,7) O20 (OH)4
Sendo Mx a representação da carga da camada do composto mineral supracitado. A massa molecular da vermiculita é aproximadamente
|
a) 780 gramas/mol.
|
|
b) 62.673 gramas/mol.
|
|
c) 71063 gramas/mol.
|
|
d) 712 gramas/mol.
|
|
e) 800 gramas/mol.
|
Os átomos ligam-se uns aos outros de diversas maneiras para "montar" todas as coisas que estão à nossa volta. O estudo da maneira em que os átomos se ligam, ou seja, das ligações químicas, é de fundamental importância para se entender as propriedades da matéria e como ela se comporta. Há dois modos principais pelos quais as ligações químicas podem ser formadas: em um deles, a ligação iônica, as partes envolvidas ("blocos construtores") encontram-se na forma de íons (possuem carga elétrica, decorrente do ganho ou perda de elétrons). Por exemplo, NaCl- sal de cozinha. Na ligação covalente, há o compartilhamento de elétrons entre dois átomos neutros. Por exemplo é o diamante, formado apenas por átomos de carbono ligados covalentemente.
Fonte:http://web.ccead.puc-rio.br/condigital/mvsl/Sala%2...
Sobre as propriedades gerais associadas a compostos iônicos e covalentes, pode-se afirmar que
|
a) compostos inorgânicos formados por ligações covalentes geralmente são formados por moléculas discretas, com ligações direcionais e as forças ligantes fortes entre os átomos da molécula.
|
|
b) a fusão de um composto iônico implica romper somente seu reticulo cristalino, o que requer certa quantidade de energia, que em geral, envolve baixas temperatura de ebulição e fusão.
|
|
c) compostos iônicos em geral conduzem a corrente elétrica, pois estando estes dissolvidos e apenas nesta condição dispersam íons migrantes para os eletrodos.
|
|
d) reações de compostos iônicos em geral são rápidas, enquanto compostos covalente reagem lentamente. Assim, estas reações ditas de covalência envolvem energia suficiente para ocorrer o processo de formação dos compostos covalentes.
|
|
e) compostos iônicos em geral são solúveis em solventes derivados da extração e beneficiamento petrolífero, ou seja, de hidrocarbonetos apolares.
|
Copyright © Tecnolegis - 2010 - 2025 - Todos os direitos reservados.
Em um recipiente de 104 mL foram colocados 0,020 mmol de pentacloreto de fósforo submetido a uma temperatura elevada, e então este composto converteu-se ao cloreto de fósforo trivalente após a decomposição térmica. O sistema em questão é reversível e tende ao equilíbrio químico. Atingida esta condição, verificou-se que a concentração do gás formado foi de 0,7 mol/L. Assim sendo, a constante de equilíbrio calculada para este processo será, aproximadamente
|
a) 0,13
|
|
b) 1,07
|
|
c) 0,38
|
|
d) 0,5
|
|
e) 1
|
Existe atualmente muita preocupação de que os aumentos antropogênicos nos gases do efeito estufa possam induzir o rápido aquecimento da superfície da Terra. Existem gases causadores do efeito estufa que ocorrem naturalmente e mostram grandes aumentos ao longo do século passado devido à atividade humana. Sobre o tema, analise as afirmativas a seguir.
I. O principal gás responsável pela geração do efeito estufa é o vapor de água troposférico. Sua concentração atmosférica provém unicamente de fontes naturais, tais como evapotranspiração e atividade vulcânica.
II. Os principais gases antrópicos são o CO2, o CH4 e o N2O.
III. Modelos matemáticos climáticos projetam que as temperaturas globais de superfície provavelmente aumentarão no intervalo entre 1,1 e 6,4°C, e o nível médio das águas do mar será consequência deste fenômeno e estará associado à redução do nível do mar, fato que trará impactos ambientais e socioeconômicos significativos para as comunidades locais.
Assinale
|
a) se todas as afirmativas estiverem corretas.
|
|
b) se somente a afirmativa I estiver correta.
|
|
c) se somente a afirmativa II estiver correta.
|
|
d) se somente as afirmativas I e II estiverem corretas.
|
|
e) se somente as afirmativas I e III estiverem corretas.
|
A figura abaixo mostra a estrutura do mineral feldspático com uma camada única visualizada perpendicular ao seu plano. A estrutura é estendida, girando cada camada sucessiva de 90°. Os feldspatos costumam ter um de cada quatro Si4+ substituído com Al3+. O desequilíbrio de carga resultante é compensado por sódio e/ou íons de potássio.
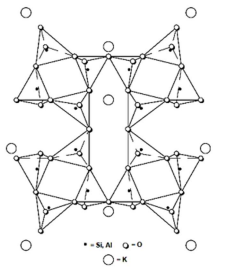
A geometria molecular predominante na estrutura, composta por átomos de silício ou alumínio é
|
a) tetraédrica.
|
|
b) angular.
|
|
c) octaédrica.
|
|
d) bipirâmide trigonal.
|
|
e) linear.
|
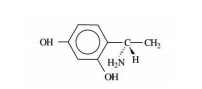
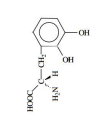
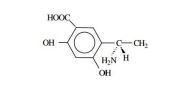
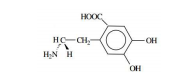
Atualmente, é possível sintetizar-se em laboratórios compostos enantioméricos que atuam como fármacos, como a Dopamina. O isômero D não possui atividade biológica, enquanto o L apresenta atividade contra o parkinsonismo. Assim, a alternativa abaixo que ilustra o enantiômero correto para a D-dopamina é
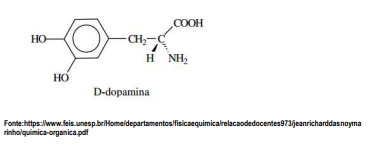
|
a)
|
|
b)
|
|
c)
|
|
d)
|
|
e)
|
Marcadores
Assinale a alternativa que contenha pelo menos um fator que não afeta a velocidade de uma reação no sentido direto.
|
a) Estado físico dos reagentes; Área de contato entre reagentes.
|
|
b) Área superficial; Concentração dos produtos.
|
|
c) Concentração dos reagentes; Presença de catalisador.
|
|
d) Temperatura da mistura reacional; Área de contato entre reagentes.
|
|
e) Presença de catalisador; Estado físico dos reagentes.
|