
 IF-PB (Instituto Federal de Educação, Ciência e Tecnologia da Paraíba) - Técnico em Laboratório - Química - IDECAN (Instituto de Desenvolvimento Educacional, Cultural e Assistencial Nacional) - 2019
IF-PB (Instituto Federal de Educação, Ciência e Tecnologia da Paraíba) - Técnico em Laboratório - Química - IDECAN (Instituto de Desenvolvimento Educacional, Cultural e Assistencial Nacional) - 2019
O potencial químico de um gás perfeito é uma função linear do logaritmo da pressão. Porém, para gases reais, esta linearidade não se verifica. Que conceito termodinâmico é utilizado para compensar esse desvio da idealidade visando manter a linearidade e um formalismo semelhante?
|
a) Entropia.
|
|
b) Entalpia.
|
|
c) Fugacidade.
|
|
d) Coeficiente de atividade.
|
|
e) Pressão parcial.
|
O efeito Joule-Thompson é definido como a variação
|
a) da temperatura de um gás quando ele sofre uma expansão isentálpica.
|
|
b) da temperatura de um gás quando ele sofre uma expansão isotérmica.
|
|
c) da temperatura de um gás quando ele sofre uma expansão isobárica.
|
|
d) do volume de um gás quando ele sofre uma expansão exotérmica.
|
|
e) do volume de um gás quando ele sofre uma compressão isotérmica.
|
“A multiplicação de uma meia-reação por qualquer número não modifica o valor do potencial-padrão de redução, E°.” Esta afirmação está correta porque
|
a) a quantidade de elétrons sempre se equivale em todas as reações.
|
|
b) a energia livre de Gibbs garante a equivalência.
|
|
c) nem E° nem E dependem da maneira como escrevemos a reação.
|
|
d) o trabalho total executado pela célula é igual em qualquer caso.
|
|
e) o trabalho por coulomb é variável.
|
Em eletroquímica, definimos potencial de junção como a
|
a) energia livre dos íons em solução.
|
|
b) mobilidade iônica.
|
|
c) constante dissociativa dos íons.
|
|
d) diferença de potencial elétrico.
|
|
e) concentração efetiva dos íons.
|
O nitrogênio (Z = 7) tem a configuração [He]2s22p1 x2p1 y2p1 z e o oxigênio (Z = 8), que aparece um orbital 2p duplamente ocupado, resulta [He]2s22p2 x2p1 y2p1 z. O conceito que explica quando os elétrons ocupam isoladamente um orbital é chamado de
|
a) Regra de Markovnikov.
|
|
b) Princípio da exclusão de Pauli.
|
|
c) Regra de Hund da máxima multiplicidade.
|
|
d) Energia da segunda ionização.
|
|
e) Entalpia-padrão de ionização.
|
A energia cinética de uma espécie em estado gasoso pode ser quantificada por um conjunto de variáveis, como tamanho das moléculas, temperatura e interação entre as moléculas. Assinale a alternativa que apresenta a equação que relaciona velocidade molecular (c) com temperatura (T).
|
a)
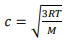 |
|
b)
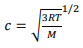 |
|
c)
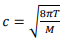 |
|
d)
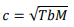 |
|
e)
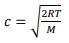 |
Liofilização ou criodessecação é um processo de desidratação em que o produto é congelado sob vácuo. A liofilização é usada na manufatura do leite em pó instantâneo, do café solúvel e por indústrias farmacêuticas. Assinale o fenômeno físico que explica a remoção de água, nessa técnica.
|
a) Condensação
|
|
b) Sublimação
|
|
c) Liquefação
|
|
d) Elevação crioscópica
|
|
e) Elevação ebulioscópica
|
O agente mais comum e mais utilizado na purificação da água na América do Norte é o ácido hipocloroso. Uma importante desvantagem do uso da cloração para desinfecção de águas é a formação de subprodutos, substâncias orgânicas potencialmente tóxicas. Assinale a alternativa que não apresenta um subproduto de cloração.
|
a) Ácidos haloacéticos
|
|
b) Trihalometanos
|
|
c) Haloacetonitrila.
|
|
d) Ácidos Húmicos
|
|
e) Clorofórmio
|
Paul Anastas e John Warner formularam os 12 Princípios da Química Verde, com o objetivo dos químicos avaliarem o impacto ambiental durante os processos químicos. Assinale a alternativa que não representa uma diretriz desses 12 Princípios.
|
a) O uso de substâncias auxiliares (solventes, agentes de separação) deve ser evitado sempre que possível.
|
|
b) Reagentes catalisadores são melhores que os reagentes usados de forma estequiométrica.
|
|
c) Metodologias analíticas precisam permitir o monitoramento e o controle em tempo real do processo para prevenir a formação de substâncias perigosas.
|
|
d) Derivatizações devem ser evitadas.
|
|
e) O Princípio 01 atribui ênfase na remediação de resíduo após ter sido produzido.
|
O ponto final de uma titulação de 5mL de uma solução de NaOH com HCl (0,2 mol.L-1 ) foi observado quando foram adicionados 20mL de HCl. Assinale a alternativa que indica corretamente a concentração obtida durante a titulação da solução de NaOH.
|
a) 0,08 mol.L-1
|
|
b) 0,4 mol.L-1
|
|
c) 0,2 mol.L-1
|
|
d) 0,8 mol.L-1
|
|
e) 0,004 mol.L-1
|